- 医療技術設備
- ITヘルスケア・遠隔医療
- モニター用ソフト
- Mia-Care Valentina Motta
管理用ソフト モニター用医療用セントラル

お気に入りに追加する
商品比較に追加する
特徴
- 機能
- 管理用, モニター用
- 応用
- 医療用
- タイプ
- セントラル
- 認証
- ISO
詳細
医療用ソフトウェア開発の簡素化
認証に必要なすべてのステップをガイドする IEC-62304 準拠のソフトウェア・スイートで、SaMD のコンセプトから実行まで。
Mia-CareのSoftware as a Medical Deviceプラットフォームにより、MedTech企業は医療用ソフトウェアのデジタル準拠ソリューションを市場に投入することができます。
次のものを取り除く
規制の落とし穴
認証取得のハードル
開発費
SaMD開発におけるMia-Careの主な特徴
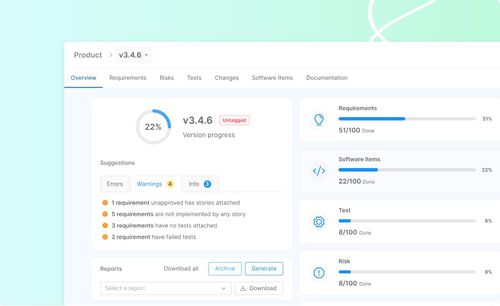
集中管理
社内開発者プラットフォームを活用し、SaMDプロジェクトの開発ステータスを一元的に確認できます。
高度な自動化
テストと技術文書作成を自動化することで、エラーを排除し、効率を向上させます。
規制遵守
ISO 13485および62304に準拠したプロセスにより、ソフトウェアのライフサイクルを管理します。
ガイド付き開発経験
SaMD開発の複雑性を排除し、開発者がソフトウェアの品質に集中できるようにします。
すべての組織レベルで価値をもたらす
開発者向け
開発者は、業界の規制や事前に定義されたソフトウェア仕様に準拠しながら、ソフトウェアライフサイクルとITインフラストラクチャを簡素化、制御、ガイドされた方法で管理できます。
プロダクトオーナー向け
製品オーナーは、製品開発の仕様とリスクを管理し、進捗と業界規制の遵守を監視し、認証機関向けの文書を管理できます。
技術リーダー向け
テクニカルリーダーは、ソフトウェアライフサイクルを通じてチームの作業をフォローし、ソフトウェアの依存関係、リリース管理、本番環境でのソフトウェアモニタリングを完全に管理できます。
---
ビデオ
カタログ
この商品のカタログはありません。
Mia-Care Valentina Mottaの全カタログを見る